آخرین شرایط ساخت واکسن های ایرانی کرونا، فخرا و کووپارس چگونه مجوز مصرف گرفتند؟
به گزارش وبلاگ مرکزی، عضو کمیته ملی واکسن کرونا ضمن تشریح آخرین اخبار پیرامون فراوری واکسن های ایرانی کرونا، گفت: تصمیمات برای پیش خرید واکسن ها یاری کننده است تا ایران به عنوان یک کشور واکسن ساز مطرح گردد؛ چراکه ثابت کردیم توانایی فراوری انواع پلتفرم های واکسن را داریم.
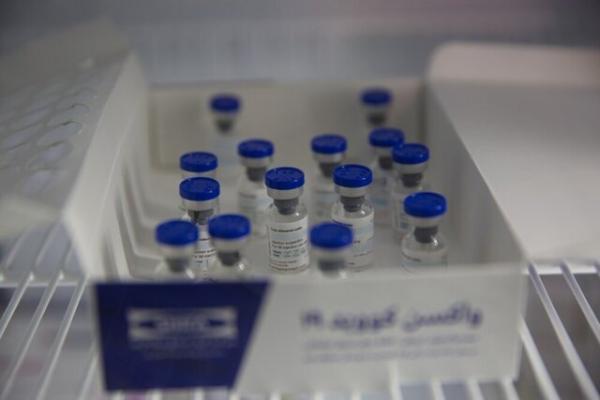
دکتر مصطفی قانعی در گفت وگو با وبلاگ مرکزی، با اشاره به اینکه اگر واکسن ها در فاز میانی فاز سوم هم نتایج موفقیت آمیز داشته باشند، اجازه ورود به بازار و مصرف اضطراری را خواهند داشت، گفت: به طور کلی وقتی واکسنی فاز یک و دو مطالعات بالینی را با موفقیت طی کند، وارد فاز سوم که مربوط به اثربخشی واکسن است، می گردد.
وی ادامه داد: دو واکسن فخرا و کووپارس در مرحله ای فاز سوم شان انجام شد که نمی توانستند از واکسن نما در مطالعه استفاده نمایند؛ بنابراین موظف بودند واکسن خود را با تزریق واکسن سینوفارم به جای واکسن نما مقایسه نمایند و در این تحقیقات باید نشان می دادند اثر بخشی واکسن شان از واکسن سینوفارم کمتر نیست که نام این نوع مطالعه نان اینفریوریتی است.
وی اضافه نمود: اگر این واکسن سازها ثابت نمایند ارزش واکسن شان از سینوفارم کمتر نیست، اجازه ورود به بازار با صدور مجوز مصرف اضطراری آنها صادر می گردد. در عین حال تا زمانی که واکسن ها تمام فاز سوم را به سرانجام نرسانند مجوز کامل برایشان صادر نمی گردد و به همین جهت فقط مجوز اضطراری صادر می گردد. واکسن های خارجی همانند سینوفارم و فایزر هم در میانه فاز 3 مجوز مصرف اضطراری گرفتند؛ اما اکنون که داده های چند 10میلیونی آنها آماده است، برای قضاوت کفایت می نماید و بنابراین می توانند مجوز سرانجامی بگیرند.
قانعی اعلام کرد: سازمان غذا و دارو به هیچ وجه نسبت به موضوعی در رابطه با دارو و واکسن کوتاهی نمی نماید و همین امر سبب شده تا محصولات بیوتکنولوژی ایرانی قابلیت صادرات دارد که علت آن هم سختگیری های حوزه غذا و دارو است.
وی اضافه نمود: ادعای مقدار فراوری واکسن کووپارس فراوری 3 میلیون دز در ماه و واکسن فخرا یک میلیون دز در ماه است اما باید دید در عمل ماهیانه چه مقدار واکسن تحویل می دهند.
عضو کمیته ملی واکسن کرونا درباره آخرین اخبار پیرامون سایر واکسن های ایرانی کرونا نیز به وبلاگ مرکزی گفت: یک هجمه ای علیه واکسن های داخلی شکل گرفت که چرا با تاخیر آمدند، شش ماه تاخیر از ابتدا داشتیم که با همان فاصله واکسن هم در حال فراوری و ورود به بازار است و واکسن کووایران برکت، پاستوکووک و... در حال ورود به بازار هستند. واکسن اسوه مجوزش از کمیته اخلاق صادر شده و باید مجوز مطالعه بالینی آن صادر گردد، پرونده واکسن MRNA شرکت رناپ تحویل سازمان غذا و دارو شده است و باید به کمیته اخلاق ارجاع داده گردد تا مجوزش صادر گردد.
وی ادامه داد: بعلاوه واکسن ایرانی - استرالیایی اسپایکوژن نیز قیمت گرفت و فکر می کنم مجوز ورود به بازار هم به زودی برای آن صادر می گردد. واکسن نورا نیز در حال طی فاز سوم است و ان شاءالله به زودی با 3 میلیون دوز فراوری در ماه وارد بازار خواهد شد.
او ادامه داد: اکنون واکسن کووپارس و اسپایکوژن را به عنوان واکسن پروتئینی و واکسن فخرا و برکت به عنوان ویروس غیرفعال شده داریم. واکسن اسوه با تکنولوژی ویروس غیرفعال و واکسن رناپ با تکنولوژی MRNA در حال طی مراحل نهایی هستند و ظرف یک ماه آینده احتمالا وارد مطالعات بالینی شوند.
او تاکید نمود: شاید ما در بهمن ماه شرایط مناسبی از نظر واکسن های داخلی داشته باشیم. نکته مهم، دیگر فناوری نیست؛ چراکه آنچه که صورت گرفته تقریبا نتایج مطلوب داده و اکنون موضوع مهم، حمایت است تا بتوانند مقدار فراوری را به حد بسیار زیادی بالا ببرند و چون فاز سوم آنها با مشکل روبرو می گردد، باید اجازه داده گردد از روش های نو برای ورود واکسن شان استفاده نمایند.
وی گفت: تصمیماتی برای پیش خرید واکسن یاری نماینده است تا ایران به عنوان یک کشور واکسن ساز مطرح گردد؛ چون ثابت کردیم توانایی فراوری انواع پلتفرم های واکسن را داریم. اگر حمایت کافی صورت گیرد سالانه یک تا 1.5 میلیارد دلار صرفه جویی ارزی خواهیم داشت.
منبع: خبرگزاری ایسنا